【CBD製品に関する法改正について】 -大麻取締法改正-

2024年12月12日に「大麻取締法及び麻薬及び向精神薬取締法の一部を改正する法律」の一部が施行されました。この法改正によってCBD製品の成分規制や販売基準が大幅に変更されると同時に、医療・ウェルネス・食品・化粧品など、CBDの活用分野がさらに拡大しています。今回のウェルネストークでは、気になる“CBDと法律のこと”を説明していきます。
大麻取締法・麻薬及び向精神薬取締法 改正の内容とは
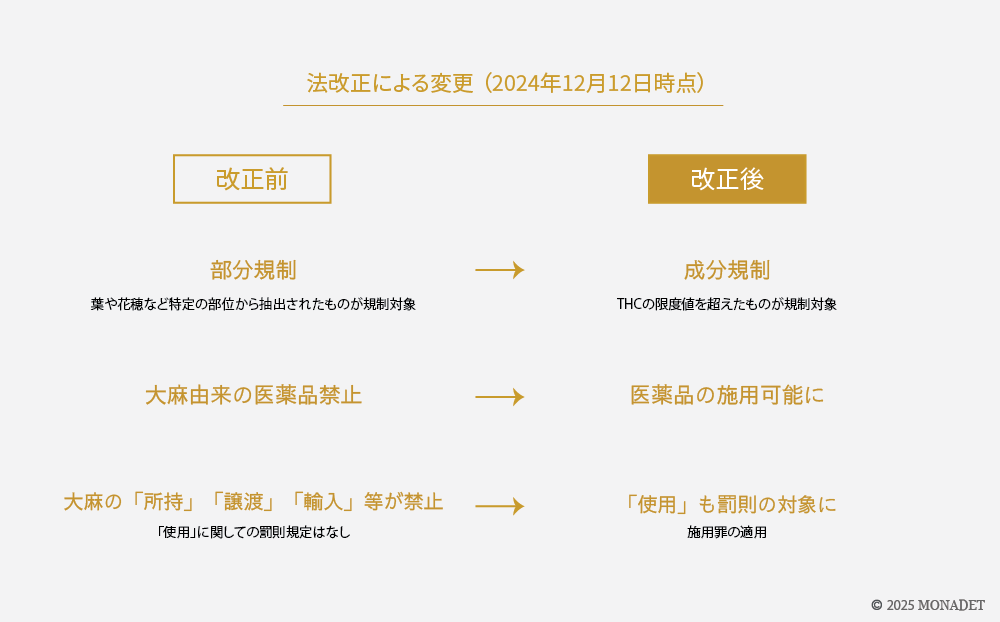
さっそく、法改正の内容から見ていきましょう。
大きく3つの変更点があります。
1.「部分規制」から「成分規制」に
これまでCBD製品は、原材料である大麻草のどの部位から成分が抽出されたかによって、規制の対象かどうかが区別されていました。
これが「部分規制」です。
例えば、茎や種子から抽出されたCBD成分はOKで、葉や花穂から抽出されたものはNG、といった具合です。
抽出元の部位に関係なく成分自体は同じであるため、この規制には実質的な意味がないとの指摘がありました。
これに対して、改正後の「成分規制」では、THC成分を含有するかどうか、が判断基準になります。
その基準として、CBD製品に残る「THCの残留限度値」が設けられました。
残留限度値とは...
THCとCBDはどちらも麻に含まれる成分であるため、CBDを抽出する際、ごく微量にTHCが含まれることがあります。その微量に残るTHCの許容値を細かく設定したものが「残留限度値」です。
この値を超えるTHCを含有する製品が、新たに日本での規制対象となりました。
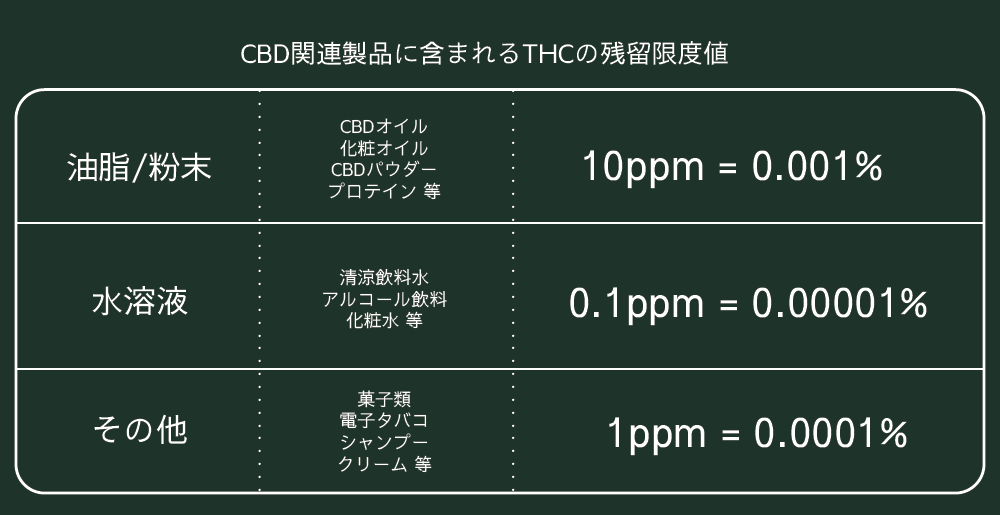
厚生労働省が示したTHC(Δ9-THC)の残留限度値は、下記の通りです(厚生労働省HPより)。
『(ア) 油脂(常温で液体であるものに限る。)及び粉末 百万分中十分の量 (10ppm、10mg/kg、0.001%)
(イ) 水溶液 一億分中十分の量(0.1ppm、0.1mg/kg、0.00001%)
(ウ) (ア)及び(イ)に掲げる物以外のもの 百万分中一分の量 (1ppm、1mg/kg、0.0001%)』
*カプセルなど粉末や液体を皮膜内に充填させたものは内容物で判断
*シート化粧品のように液体に浸潤させたものは液体
製品の種類によってその値が変わりますが、THCの残留限度値は0.001%から0.00001%。
米国の基準値である0.3%と比べると、限りなく低い数値に定められたことがわかります。
2.大麻由来の医薬品が施用可能に
これまでは大麻草から製造された医薬品の「施用、交付、受施用の禁止規定」がありました。
つまり、大麻由来の成分を医療目的で使うことはできませんでした。
しかし、CBDの有用性が認められた今、
“一般で使用できるCBD製品があるのだから、「医薬品」としてもCBDを活用できるようにしよう” ということになりました。
米国や英国、EUなどではてんかんの発作を抑える薬にCBDが使われています。
実は日本でも、今回の法改正に先立ち、CBDを主成分とする医薬品の治験が行われていました。
こうした背景を踏まえ、「大麻由来の医薬品が施用可能」*になったのです。
*施用・・・薬や医薬品を身体に投与・服用すること
この決定により、THCに関しても医薬品としての禁止規定が削除されました。
これらの大麻由来成分が医薬品として承認され、日本の医療現場で活用される日も近いのではないでしょうか。
3.不正使用の罰則強化
これまでは、大麻(THC)の「所持」「譲渡」「輸入」などが禁止されていましたが、新たに「使用」も禁止されました。
近年若年層による不正使用が目立つことを受け、その拡大を防ぐ目的で見直されたものです。
CBD製品についても、先ほどの「残留限度値」を超えるTHCが含まれた製品の使用は違法となり、施用罪が適用されます。
THCとCBDはどちらも麻から採れる成分と説明しましたが、国内での使用規制はもちろん、成分そのものの性質にも大きな違いがあります。
次に、THCとCBDの違いについて見ていきましょう。
THCとCBDの違い
日本で規制されているTHC、規制されていないCBD
同じ大麻草に含まれるこの2つの成分には大きな違いがあります。
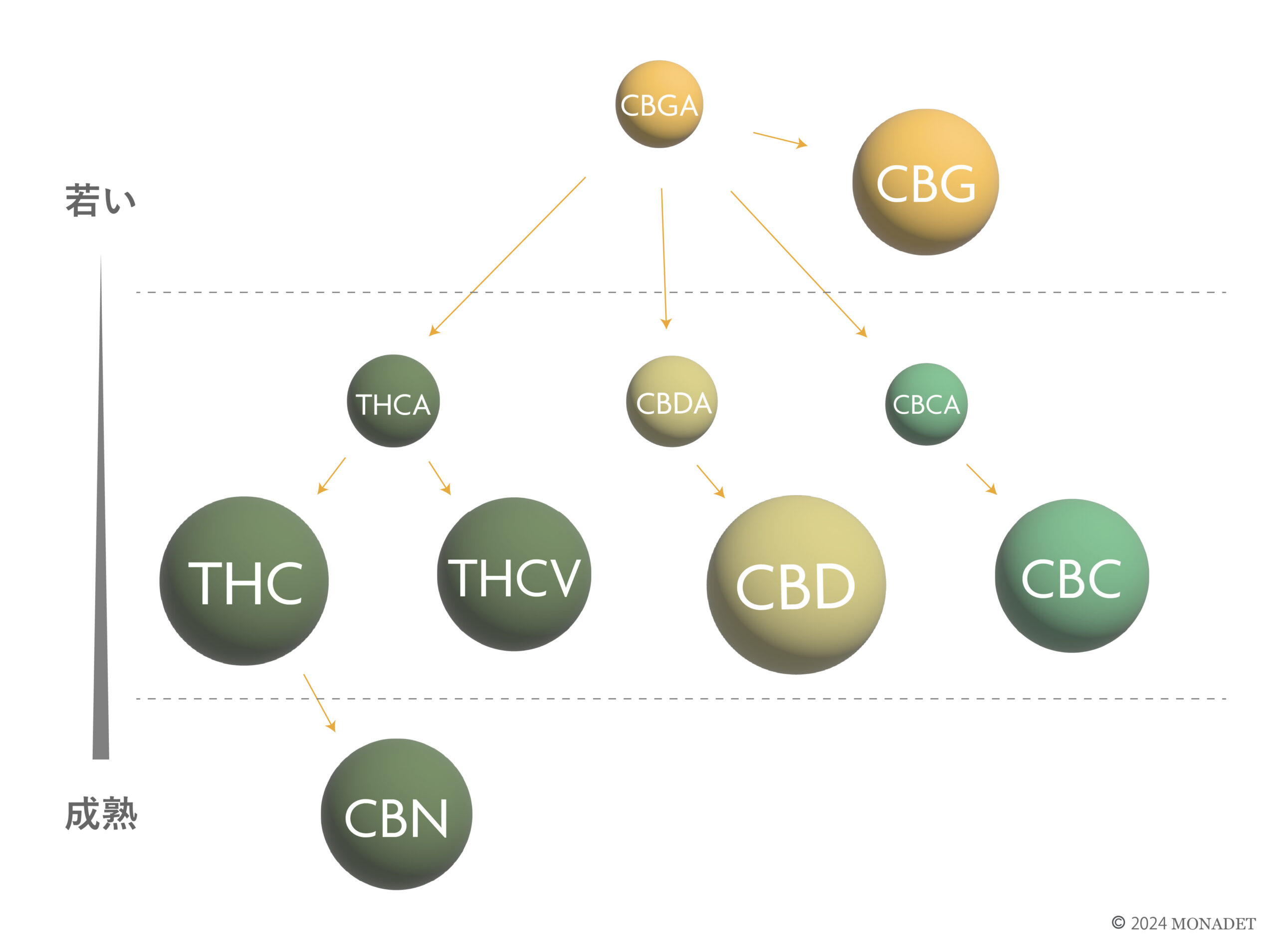
どちらも「カンナビノイド」と呼ばれる、麻由来の成分に分類されるのですが、カンナビノイドにはTHCやCBDの他にも、「CBG」や「CBN」など100を超える種類があります。
そして面白いことに、これらのカンナビノイドは、それぞれ異なる特性を持っています。
THCとCBDにおいても、私たちの体内で作用するメカニズムが異なり、心身に与える影響も違うのです。
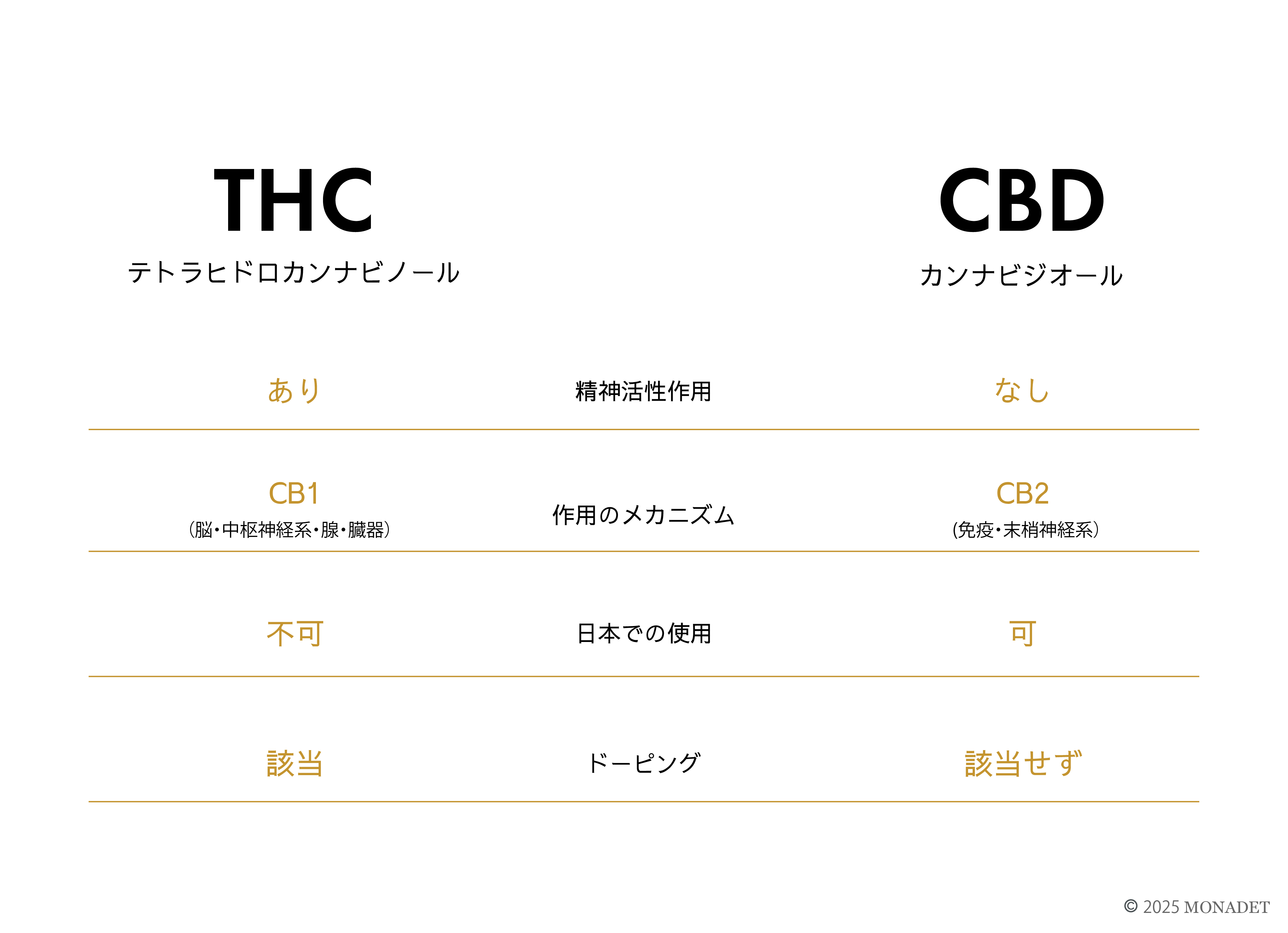
THC(テトラヒドロカンナビノール)
THCは、精神活性作用を持つ、ということが大きな特徴です。
私たちの体内にある「CB1」という受容体に結合することで、神経系に直接作用します。
これによって高揚感など感覚の変化が生じるのですが、この作用が危険視され、日本では規制の対象となっています。
今回の法改正では、THCの使用に対する罰則規定が加わったほか、CBD製品に微量に含まれるTHCについても明確な基準が示されるなど、規制が厳格化されました。
一方で、米国の一部の州やカナダ、オランダ、タイなど、THCを含む製品の販売・使用が許可されている地域もあります。
そのため、海外で購入したCBD製品を日本に持ち込もうとする場合には注意が必要です。
CBD(カンナビジオール)
CBDは精神活性作用を持たず、主に免疫や末梢神経系に働きかけます。
ドーピングにも該当しないことから、怪我のケア、回復促進、パフォーマンス向上といった目的でCBDを使用するアスリートも増えています。
一般的にはストレス緩和、リラックス、睡眠の質向上など、幅広い目的で使用されています。
CBDのこれまでの道のり

2018年頃から認知度が高まってきたCBD。
世界保健機関(WHO)が
「依存や乱用の可能性がなく、国際的な薬物条約の規制対象外」と発表したことを皮切りに、世界アンチ・ドーピング機構もCBDを禁止物質リストから除外するなど、その安全性が国際的に認められてきました。
また、同年にCBD製剤「エピディオレックス」が米国で初めて医薬品として承認され、
難治てんかんの治療薬として使われています。
実は、日本国内でもCBDを医療に取り入れる動きは、既に始まっています。
2022年にはCBD製剤の治験が始まり、
2024年には「希少疾病用医薬品」*として指定され、本格的にその活用に向けて動き出しています。
*希少疾病用医薬品・・・医療上の必要性が高いにもかかわらず、患者数が少ないことにより研究開発が進まない医薬品及び医療機器の開発を支援することを目的とするもの。
世界初のCBD医薬品「エピディオレックス」
エピディオレックスは、アメリカで開発された、CBDを主成分とする処方薬です。
大麻草由来であるCBDを主成分とする薬として、世界で初めて承認されたものです。
主にドラヴェ症候群やレノックス・ガストー症候群といった、難治てんかんの患者の発作を抑制するために使われています。
CBDが持つ神経保護作用がてんかん発作を軽減すると考えられ、体への負担も少ないことから、その有用性と安全性が高く評価されています。
日本国内での治験も始まっており、これから医療での活用が進んでいくでしょう。
CBDのこれから

CBDをはじめとする大麻草由来製品の活用が広がる中、「大麻草の栽培」に関しても新たな動きがあります。
厚生労働省が今回発表した法改正の内容には、大麻草の栽培に関する免許制度の見直しや新たな制度の導入も盛り込まれました。
麻は古くから繊維や建材としても利用されており、これに加え、CBD製品として食品や化粧品、そして医薬品への活用も進む中で、国内での生産力を向上させることが重要視されています。
この見直しが日本の産業にどのような影響を与えるのか、今後の動向に注目が集まります。
流行を超え、ヘルシーな選択肢として
CBDは医療に限らず、日々の健康習慣として自分で取り入れられるものです。
CBD入りのドリンクやスイーツ、化粧品や健康食品などを見かけたことがある方も多いのではないでしょうか。
今回の法改正で、製品に含まれるTHCの限度値が明確になりました。
世界有数の厳しい規格に基づいて生産される日本のCBD製品は、これまで以上に安心して使用できるものになるでしょう。
より良い製品を選ぶためには、含まれるCBD原料の規格を確認することも大切です(メーカーに問い合わせると「COA」と呼ばれる、成分の分析結果を提示してもらうことができます)。
その多様な働きに対して副作用がほとんどないCBDは、正しく取り入れることで、きっと私たちに良い影響を与えることでしょう。
MONADETは、よりヘルシーな社会の実現を目指し、品質と安全性にこだわったウェルネスアイテムをお届けします。



